Масса газа – физическая величина, которая является одним из основных параметров, определяющих его свойства и поведение. Определение массы газа играет важную роль в химии, физике и других науках, где газы широко используются и изучаются.
Существуют различные методы и приборы, которые позволяют определить массу газа с высокой точностью. Одним из самых распространенных методов является взвешивание. Для этого используются взвески или весы с высокой точностью, которые позволяют измерить массу газа с большой точностью.
Другим методом определения массы газа является использование уравнения состояния идеального газа. Это уравнение позволяет связать массу газа с другими его параметрами, такими как давление, объем и температура. Таким образом, зная значения этих параметров, можно определить массу газа.
Для более точного определения массы газа часто применяются специальные приборы, такие как газовые счетчики, микровесы, пирометры и другие. Эти приборы обладают высокой точностью и позволяют определить массу газа с большей точностью, чем обычные взвески.
Определение массы газа в химии

Существуют различные методы, которые позволяют определить массу газа. Во-первых, в химической лаборатории широко используется аналитические весы. С их помощью можно точно измерить массу газа в закрытой системе, а также провести взвешивание реагентов перед проведением реакции.
Второй метод - гравиметрический анализ - основывается на измерении массы веществ, образующегося или исчезающего в реакции. Такой метод используется в ряде газоаналитических приборов, например, в газохроматографах и спектрометрах масс-спектрометров.
Третий метод - объемный анализ - основывается на измерении объема газа и его плотности. Измерение объема может быть выполнено различными методами, например, с использованием газовых сильфонных баллонов или мерной колбы. Плотность газа можно определить с помощью плотномеров и гидростатических весов.
В зависимости от конкретной задачи и доступности приборов, можно выбрать наиболее удобный и точный метод определения массы газа. Определение массы газа в химии является неотъемлемой частью большинства лабораторных исследований, обеспечивая точность и достоверность результатов.
Использование газовых мер

Определение массы газов часто требует использования специальных газовых мер и приборов.
Одним из наиболее распространенных методов измерения массы газа является использование газовых шприцов. Газовый шприц представляет собой цилиндр с поршнем, который можно двигать внутри цилиндра. При измерении массы газа с помощью газового шприца, газ помещается внутрь шприца, а затем поршень перемещается так, чтобы объем газа уменьшился до известной отметки. Зная объем газа и его давление при заданной температуре, можно рассчитать массу газа с помощью уравнения состояния газа.
Другим распространенным прибором для измерения массы газа является газовый счетчик. Газовый счетчик устанавливается на трубопроводе и позволяет измерять объем газа, проходящего через него. Обычно газовый счетчик имеет шкалу, на которой можно видеть текущий объем газа. Путем умножения объема газа на его плотность при заданной температуре и давлении можно рассчитать массу газа.
Использование газовых мер и приборов позволяет определить массу газа с высокой точностью и надежностью, что является важным при проведении химических экспериментов и производственных процессов.
Метод взвешивания газовых смесей

Метод взвешивания газовых смесей широко используется в химии для определения массы газа. Он основан на принципе измерения изменения массы системы в результате взаимодействия газа с реагентом или адсорбентом.
Для проведения взвешивания газовых смесей необходимы специальные приборы, такие как аналитические весы или гравиметры. Эти приборы позволяют точно измерять изменение массы системы при взаимодействии газа с реагентом.
Процесс взвешивания газовых смесей состоит из нескольких этапов:
- Подготовка аналитических весов или гравиметра путем их калибровки и проверки точности измерений.
- Проведение реакции или адсорбции газовой смеси с использованием реагента или адсорбента.
- Измерение изменения массы системы с помощью аналитических весов или гравиметра.
Полученные данные массы газа позволяют определить его содержание в газовой смеси. Для более точного результата необходимо учитывать дополнительные факторы, такие как давление, температура и влажность газа.
Метод взвешивания газовых смесей является одним из наиболее надежных и точных способов определения массы газа в химии. Он находит широкое применение в различных областях, включая аналитическую химию, физическую химию и промышленные процессы.
| № | Масса до реакции (г) | Масса после реакции (г) | Изменение массы (г) |
|---|---|---|---|
| 1 | 10.05 | 9.72 | -0.33 |
| 2 | 12.10 | 11.83 | -0.27 |
| 3 | 8.75 | 8.42 | -0.33 |
Использование газовых баллонов

Газовые баллоны широко используются в химических лабораториях для хранения и переноса различных газов. Они представляют собой металлические цилиндры, которые могут быть заполнены различными газами, такими как кислород, азот, водород и другие.
Для использования газовых баллонов необходимо применять специальные приборы, такие как редукторы давления и расходомеры. Редукторы давления позволяют уменьшить высокое давление газа в баллоне до необходимого уровня для работы с ним. Расходомеры, в свою очередь, используются для измерения расхода газа и контроля его давления.
Перед использованием газового баллона необходимо провести проверку его целостности и наличия правильной маркировки, указывающей на содержимое баллона. Перед подключением баллона к приборам необходимо также проверить, что все соединения надежно закреплены и герметичны.
При использовании газовых баллонов необходимо соблюдать меры безопасности, так как газы могут быть опасными при неправильном обращении. Необходимо работать в хорошо проветриваемом помещении или в вытяжной шкафу, чтобы избежать возможного отравления газами. Также необходимо использовать защитные средства, такие как защитные очки и перчатки, чтобы избежать возможного контакта с газом.
Термоанемометр в определении массы газа

Для определения массы газа с помощью термоанемометра используется следующая методика. Первоначально термоанемометр калибруется с использованием стандартного газа или известной массы газа. Затем производится измерение скорости потока газа, при котором термоэлементы термометра достигают установившегося значения температуры.
Зная скорость потока и исходную калибровку термоанемометра, можно определить массу газа с помощью соответствующих расчетов. Это основывается на предположении, что скорость потока газа пропорциональна массе газа.
Преимущества термоанемометра в определении массы газа включают простоту использования, точность измерений и возможность работы с различными типами газов. Также данный метод не требует дополнительных сложных устройств и особых условий эксплуатации.
Однако следует отметить, что термоанемометр может быть подвержен ошибкам из-за влияния окружающей среды. Также необходимо учитывать факторы, такие как температура и давление газа, которые могут влиять на точность измерений. Поэтому рекомендуется проводить калибровку термоанемометра перед каждым измерением для достижения наибольшей точности результатов.
Метод циклического расширения газа
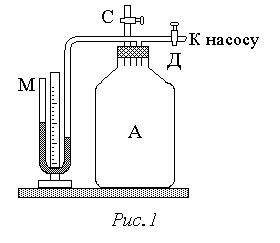
В процессе циклического расширения газа, сначала небольшое количество газа заполняет капилляр или тонкостенную трубку с известной площадью поперечного сечения. Затем газ перегоняется через градуированный сосуд, где его давление и объем измеряются.
Далее, газ снова возвращается в начальную фазу, и процесс повторяется несколько раз для получения более точных результатов. Во время расширения и сжатия газа происходит перемещение поршня, который проводит работу над газом и изменяет его объем.
Исходя из полученных данных о давлении и объеме газа в каждой фазе цикла, можно применить закон Бойля-Мариотта для определения массы газа. Расчеты основаны на принципе сохранения энергии, где работа, совершенная над газом, равна работе, совершенной газом.
Метод циклического расширения газа широко используется в химических и физических лабораториях для определения массы различных газов, включая воздух, углекислый газ и азот.
Использование капиллярных газомеров

Капиллярные газомеры состоят из главной камеры, капиллярной трубки и специального устройства для измерения давления. Давление газа внутри газомера изменяется в зависимости от количества газа, проходящего через капиллярную трубку. С помощью устройства для измерения давления можно определить массу газа.
Использование капиллярных газомеров имеет ряд преимуществ. Во-первых, эти приборы позволяют получать точные и надежные результаты. Во-вторых, капиллярные газомеры отличаются высокой чувствительностью, что позволяет измерять массу газа в малых количествах. Кроме того, капиллярные газомеры обладают удобством использования и не требуют сложной калибровки.
Одним из распространенных примеров капиллярных газомеров является Гольджемсов газомер. В этом приборе газ проходит через капиллярную трубку с помощью разрежения, создаваемого вакуумным насосом. Степень разрежения контролируется с помощью специального манометра.
Таким образом, использование капиллярных газомеров является важным методом для определения массы газа в химии. Эти приборы позволяют получать точные результаты и имеют широкий спектр применения в химической лаборатории.
Метод абсорбции газов

Принцип работы метода абсорбции газов заключается в выборе абсорбента, то есть вещества, способного химически связывать и удерживать исследуемый газ. В процессе поглощения газа абсорбент изменяет свою массу, что позволяет определить массу поглощенного газа.
Для проведения эксперимента с использованием метода абсорбции газов необходимо следующее оборудование:
- Реакционная камера - специальное устройство, в котором происходит взаимодействие газа и абсорбента.
- Абсорбент - вещество, способное поглощать и удерживать газ.
- Капилляр или переносная мембрана - используется для подачи газа в реакционную камеру или для разделения газовой смеси на отдельные компоненты. Это позволяет провести определение массы конкретного газа.
- Приборы для измерения массы - весы или другие устройства, которые позволяют определить массу абсорбента с поглощенным газом.
Метод абсорбции газов широко используется в химической аналитике для определения содержания определенного газа в смеси. Это важный метод, который позволяет получить точные результаты и различные параметры химических реакций, которые могут быть использованы в многих областях науки и промышленности.
Газовый сообщающий сосуд
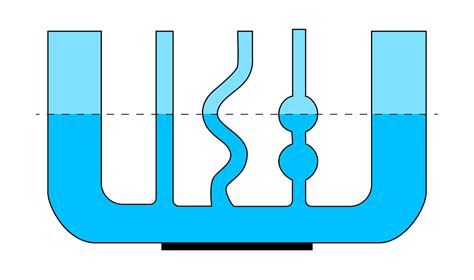
Перед использованием газового сообщающего сосуда необходимо убедиться, что все соединения герметичны, чтобы исключить утечку газа. Затем в одну из частей сосуда помещается измеряемое количество газа, например, путем заполнения его при постоянном давлении или объеме.
После этого происходит перенос газа через трубки или краны в другую часть сосуда. Объем и давление газа в каждой части сосуда могут быть измерены с помощью специальных мерных приборов, таких как манометр и градуированная пробка.
Затем происходит сравнение объема и давления газа в каждой части сосуда. По закону Гей-Люссака можно установить соотношение между начальным объемом и давлением газа и его конечным объемом и давлением. Из этих данных можно определить молекулярную массу газа.
Газовый сообщающий сосуд является важным инструментом для проведения экспериментов с газами в химической лаборатории. Он позволяет точно измерять массу газа и проводить различные расчеты и анализы, необходимые для изучения свойств и поведения газовых веществ.
Ультрафиолетовый спектрофотометр в определении массы газа

Принцип работы ультрафиолетового спектрофотометра основан на законе Бугера-Ламберта, который устанавливает линейную зависимость между абсорбцией света и его концентрацией вещества. Ультрафиолетовый свет взаимодействует с молекулами газа, вызывая переход электронов на более высокие энергетические уровни.
Ультрафиолетовый спектрофотометр состоит из источника света, монохроматора, образцовой камеры и детектора. Источник света излучает ультрафиолетовое излучение с определенной длиной волны. Затем свет попадает на образец газа в камере, где происходит его абсорбция. После прохождения через образец свет попадает на детектор, который регистрирует интенсивность прошедшего через образец света.
С помощью ультрафиолетового спектрофотометра можно определить массу газа, используя калибровочную кривую. Для этого необходимо провести измерение абсорбции известных растворов газа с различными концентрациями и построить график зависимости абсорбции от концентрации. Затем, измеряя абсорбцию неизвестного образца газа, можно определить его концентрацию и массу.
Ультрафиолетовый спектрофотометр позволяет проводить измерения с высокой точностью и чувствительностью. Он широко используется в химическом и биологическом анализе для определения концентрации различных веществ, в том числе газов. Этот прибор существенно упрощает и ускоряет процесс определения массы газа и позволяет получить более точные результаты.