Ионная связь - один из основных типов химических связей между атомами. Она возникает между атомами с разными степенями электроотрицательности. Ионная связь - это процесс образования ионов, положительно и отрицательно заряженных частиц, и их последующего притяжения друг к другу. Важно понимать, что ионная связь является результатом обмена электронами между атомами и формирования электрических зарядов.
Принципы образования ионной связи лежат в основе ионной теории. По этой теории, атомы сильно отличающихся по электроотрицательности элементов имеют разные способности притягивать электроны к себе. Электроотрицательные элементы, такие как кислород, флуор, хлор, обладают большей силой притяжения электронов, чем элементы с низкой электроотрицательностью, такие как натрий, калий, магний.
Пример образования ионной связи:
Возьмем, например, образование ионной связи между металлическим натрием (Na) и неметаллическим хлором (Cl). Атомы натрия имеют один электрон во внешней электронной оболочке, в то время как атомы хлора имеют семь электронов во внешней оболочке. Ионная связь образуется, когда атом натрия отдает свой единственный электрон атому хлора. В результате этого происходит образование положительно заряженного натрия (Na+) и отрицательно заряженного хлора (Cl-). Заряды притягиваются друг к другу, образуя кристаллическую решетку ионного соединения - хлорид натрия (NaCl).
Принцип образования ионной связи в химии

Процесс образования ионной связи происходит при взаимодействии металлических и неметаллических элементов. Неметаллы обладают большой электроотрицательностью, что позволяет им сильно притягивать электроны. Металлы же обладают низкой электроотрицательностью, что означает, что у них есть возможность отдавать электроны.
Неметаллы отдают внешние электроны металлам, чтобы достичь стабильной октаэдрической конфигурации, имеющей 8 электронов на внешнем энергетическом уровне. В результате, неметаллы образуют отрицательно заряженные ионы. Металлы же получают эти электроны и образуют положительно заряженные ионы.
Поскольку ионы разного заряда притягиваются друг к другу, они образуют кристаллическую решетку. Эта решетка сохраняет электронейтральность, так как положительные ионы равны по численности отрицательным ионам.
Примерами веществ, образующих ионные связи, являются хлорид натрия (NaCl), сульфат калия (K2SO4) и оксид магния (MgO).
Какие элементы способны формировать ионную связь

Ионные связи образуются между элементами, которые имеют различные электроотрицательности.
Наиболее распространенными элементами, способными формировать ионные связи, являются металлы и неметаллы. Металлы, обычно, имеют низкую электроотрицательность и готовы отдавать электроны. Неметаллы, в свою очередь, имеют высокую электроотрицательность и обладают способностью принимать электроны.
Примерами элементов, способных образовывать ионные связи, являются натрий (Na) и хлор (Cl). В процессе образования ионной связи натрий отдает электрон неметаллу - хлору, что приводит к образованию иона натрия (Na+) и иона хлора (Cl-). Эти ионы притягиваются друг к другу и образуют кристаллическую решетку, составляющую хлорид натрия (NaCl).
Ионные связи также могут образовываться между другими парами элементов, например, между калием (K) и бромом (Br), магнием (Mg) и фтором (F) и т.д. Все эти связи основаны на принципе передачи электронов от металла к неметаллу.
Итак, элементы, способные формировать ионные связи, обладают разными электроотрицательностями и могут передавать или принимать электроны, чтобы достичь равновесия электронной оболочки. Ионные связи существуют во множестве химических соединений, таких как соли, оксиды и галогениды.
Процесс образования ионной связи

Процесс образования ионной связи можно описать следующим образом:
- Атомы, вступающие в реакцию, имеют различную электроотрицательность – способность притягивать электроны.
- В результате этого различия, один из атомов становится электроотрицательным, а другой – электроположительным.
- Электроотрицательный атом притягивает электроны к себе, что приводит к образованию отрицательного иона (аниона).
- Электроположительный атом отдает электроны, образуя положительный ион (катион).
- Образовавшиеся ионы притягиваются друг к другу благодаря противоположным зарядам и образуют ионную связь.
Процесс образования ионной связи можно наблюдать на примере образования солей. Например, когда натрий (Na) реагирует с хлором (Cl), образуется ионный кристалл хлорида натрия (NaCl):
| Реагент | Ионная формула |
|---|---|
| Натрий | Na |
| Хлор | Cl |
| Хлорид натрия | NaCl |
В данном случае, натрий (Na) отдает один электрон хлору (Cl), образуя катион Na+, а хлор (Cl) принимает этот электрон, образуя анион Cl-. Эти ионы притягиваются друг к другу и образуют кристаллическую решетку хлорида натрия.
Таким образом, процесс образования ионной связи основан на перераспределении электронов между атомами с различной электроотрицательностью, что приводит к образованию ионов и их последующей связи в ионную решетку.
Особенности и структура ионной связи

Структура ионной связи представляет собой решетку, в которой ионы положительного и отрицательного зарядов располагаются в определенном порядке. В ионных соединениях положительные ионы называют катионами, а отрицательные – анионами.
В ионной связи каждый ион окружен своими противоположно заряженными ионами. Наиболее распространенной структурой ионной связи является решетка, в которой катионы и анионы образуют равномерную сетку. Каждый катион окружен анионами, а каждый анион окружен катионами.
Структура ионной связи не только обеспечивает стабильность соединения, но и определяет его физические и химические свойства. Например, размер иона и его заряд влияют на величину энергии ионной связи и температуру плавления соединения.
Важно отметить, что в ионных соединениях ионная связь является несмещаемой – при нарушении структуры решетки соединение может распадаться на отдельные ионы. Также структура ионной связи может изменяться при изменении условий, например при повышении температуры или изменении окружающей среды.
Кристаллическая решетка ионных соединений
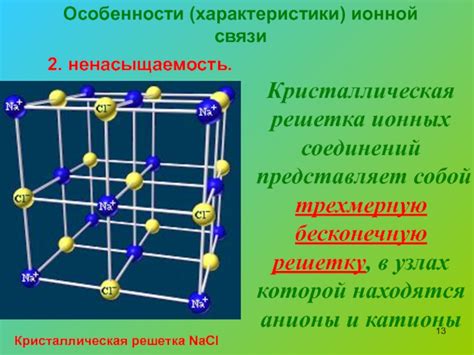
Каждый ион в ионной решетке окружен определенным числом атомов другого заряда. Положительные ионы (катионы) окружены отрицательными ионами (анионами), а отрицательные ионы окружены положительными ионами. Это создает баланс зарядов и поддерживает стабильность ионной решетки.
Структура кристаллической решетки ионных соединений указывает на их характерные свойства. Например, ионные соединения обладают высоким плавлением и кипением, так как требуется большое количество энергии для разрушения электростатических связей в решетке. Они также обладают электропроводностью только в расплавленном или растворенном состоянии, так как ионы связаны в кристаллической решетке и не могут свободно перемещаться.
Примеры ионных соединений с разными типами решеток:
1. Натрий хлорид (NaCl): этот ионный соединение имеет кубическую решетку, где каждый натриевый ион окружен шестью хлоридными ионами, а каждый хлоридный ион окружен шестью натриевыми ионами.
2. Магний оксид (MgO): этот ионный соединение имеет кубическую решетку, где каждый магниевый ион окружен шестью оксидными ионами, а каждый оксидный ион окружен шестью магниевыми ионами.
3. Аммоний хлорид (NH4Cl): этот ионный соединение имеет тетрагональную решетку, где каждый аммониевый ион окружен четырьмя хлоридными ионами, а каждый хлоридный ион окружен четырьмя аммониевыми ионами.
Примеры ионных соединений

Ионные связи широко распространены в химических соединениях. Некоторые из наиболее известных примеров ионных соединений включают:
1. Хлорид натрия (NaCl): Это одно из самых распространенных ионных соединений. Хлорид натрия образуется из ионов натрия (Na+) и хлора (Cl-) и является основной составной частью поваренной соли.
2. Сульфат магния (MgSO4): Это ионное соединение образуется из ионов магния (Mg2+) и сульфата (SO42-). Сульфат магния широко используется в медицине и сельском хозяйстве.
3. Карбонат кальция (CaCO3): Это ионное соединение образуется из ионов кальция (Ca2+) и карбоната (CO32-). Карбонат кальция является основным компонентом мрамора и известняка.
4. Гидроксид алюминия (Al(OH)3): Это ионное соединение образуется из ионов алюминия (Al3+) и гидроксида (OH-). Гидроксид алюминия используется в производстве алюминия и водоотведении.
5. Фосфат аммония (NH43PO4): Это ионное соединение образуется из ионов аммония (NH4+) и фосфата (PO43-). Фосфат аммония используется в удобрениях и в растворах для стекла.
Это лишь несколько примеров ионных соединений, которые широко распространены и имеют важное значение в различных областях человеческой деятельности.
Значение ионной связи в химических реакциях

Ионная связь играет важную роль в процессах химических реакций. Это особый тип химической связи, который формируется между ионами положительного и отрицательного заряда.
Ионная связь возникает из-за электростатического притяжения между ионами с противоположным зарядом. Положительные ионы (катионы) притягивают отрицательные ионы (анионы), образуя устойчивые междуатомные связи.
Важно отметить, что ионная связь характерна для соединений, состоящих из металлов и неметаллов. Металлы обычно отдают электроны и образуют положительные ионы, а неметаллы принимают эти электроны и образуют отрицательные ионы. Такое электронное перераспределение позволяет образовать стабильные ионные соединения.
Ионная связь имеет ряд важных применений и значений в химических реакциях. Она является ключевым фактором в формировании солей, кислот и оснований. Ионные связи между ионами катионов и анионов делают эти соединения устойчивыми и способными участвовать в различных химических превращениях.
Кроме того, ионная связь имеет особое значение в электролитических реакциях, где ионы разделяются под действием электрического тока. В таких реакциях ионное соединение распадается на положительные и отрицательные ионы, что позволяет проводить электрический ток.
Таким образом, ионная связь имеет огромное значение в химических реакциях, регулируя стабильность и реакционную способность соединений. Понимание принципов и механизмов образования ионной связи позволяет получать новые материалы с улучшенными свойствами и участвовать в различных технологических процессах.